Maddenin en küçük yapı birimi atomlardır. Atomlar birleşerek maddeleri meydana getirir. Kimyasal ve fiziksel olaylar, elementlerin ve bileşiklerin etkileşimleri sonucu oluşur. Kimyasal denklemleri ifade ederken daha basit olması açısından ortak ve anlaşılır bir dil oluşturulmuştur. Aynı cins atomlardan oluşan saf maddelere element denir. En küçük yapıtaşı atom olanlara atomik element, molekül olanlara moleküler element denir.
Element Sembolleri ve Adları
Aynı proton sayısına sahip tek tür atomlar topluluğuna element denir. Örneğin
O2 elementi oksijeni simgeler.- Elementler saf ve homojenlerdir.
- Fiziksel veya kimyasal yöntemlerle daha basit bileşenlere parçalanamazlar.
- Belirli ayırt edici özellikleri vardır( erime noktası, kaynama noktası, yoğunluk gibi)
- Semboller ile gösterilirler.
- 118 element vardır. Bunların 92 tanesi doğal, diğerleri yapaydır.
- Monoatomik elementler doğada tek atomlu halde bulunan elementlerdir. Soygazlar bu gruba girer. He,Ne,Ar,Kr bu tip elementlere birer örnektir.
- Diatomik elementler doğada ikili moleküller halinde bulunan elementlerdir. Cl₂, H₂, O₂, N₂ bu tip elementlere örneklerdir.
- Poliatomik elementler ise doğada ikiden fazla atom içeren moleküller halinde bulunan elementlerdir. S₈ ve O₃ bu tip elementlere örnektir.
- Elementlarin çoğu bileşiklerin kimyasal yöntemler ile ayrışması sonucu elde edilir.
Elementleri sembolle göstermeyi ilk uygulayan kişi J.J.Berzelius’tur. Elementlerin monoatomik gösterimleri semboldür, moleküler gösterimleri formüldür. Örneğin Fe, Cu, Cl, Ne, Ag, K, P gibi gösterimler monoatomik gösterimdir ve semboldür. N2, Cl2, O2 gibi gösterimler ise formüldür.
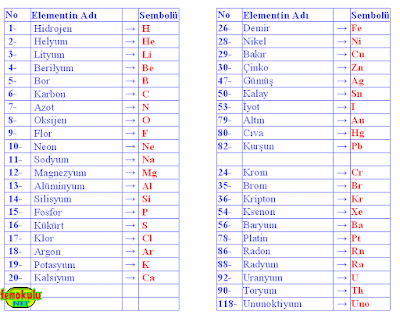
Aşağıdaki tabloda bazı elementlerin adları ve sembolleri verilmiştir.
| Element Adı | Element Sembolü |
|---|---|
| Hidrojen | H |
| Helyum | He |
| Lityum | Li |
| Berilyum | Be |
| Bor | B |
| Karbon | C |
| Azot | N |
| Oksijen | O |
| Flor | F |
| Neon | Ne |
Elementler metal, ametal ve soygazlar olmak üzere 3 sınıfa ayrılır.
- Metaller; parlaktır, elektriği iletebilirler, metallere şekil verilebilir ve oda sıcaklığında genellikle (civa sıvı) katı halde bulunurlar.
- Ametaller; mattır, elektriği iletmez ve kırılgandırlar; oda sıcaklığında katı, sıvı veya gaz halde bulunabilirler.
- Soygazlar; oda sıcaklığında hepsi gaz halinde bulunur, kararlıdırlar, bileşik yapmazlar, Helyum, Neon, Argon, Kripton, Ksenon ve Radon olmak üzere altı tanedirler.
Bileşikler
Bileşik, iki ya da daha fazla cinste atomun belirli oranda bir araya gelerek oluşturduğu saf maddelere denir. Elementlerden farklı cins atomlar içerirler. Örneğin su (2 hidrojen atomuyla 1 oksijen atomunun birleşmesiyle oluşmuş) bir bileşiktir.
- Bileşikler tek tür tanecikten oluşmaktadır.
- Saf maddelerdir.
- Hal değişimi dışında homojen maddelerdir.
- Yapısındaki elementlerin özelliklerini göstermezler.
- En az 2 farklı tür atom içerirler.
- Ayırt edici özellikleri vardır.
- Fiziksel yöntemlerle daha basit bileşenlerine ayrıştırılamazlar fakat kimyasal yöntemlerle ayrıştırılabilirler.
- Bileşikler formüller ile gösterilir.
- Bileşiği oluşturan elementler arasında belirli bir oran vardır. Suda hidrojen atomunun oksijen atomuna oranı 2’dir.
Bazı Bileşiklerin Yaygın Adları
| Bileşik Fomüllü | Yaygın Adı |
|---|---|
| H2O | Su |
| HCl | Tuz ruhu |
| H2SO4 | Zaç yağı |
| CaCO3 | Kireç taşı |
| NaHCO3 | Yemek sodası |
| NH3 | Amonyak |
| NaOH | Sud kostik |
| CaO | Sönmemiş kireç |
| NaCI | Yemek Tuzu |
Bazı Bileşiklerin Kimyada Kullanılan Adları
- CO = Karbon monoksit
- CO2 = Karbon dioksit
- NO = Azot monoksit
- N2O = Di azot monoksit
- NO2 = Azot dioksit

Hiç yorum yok:
Yorum Gönder
ders,plan,proje,performans,ödev